Determinación de glucosa
C. Menor-Salván v1. 2026
Esto hace referencia a nuestra práctica en Bioquímica de la Universidad de Alcalá, sobre determinación del glucógeno hepático y valoración cuantitativa de la glucosa. Se hacen referencia a datos y contenido dle guión de la práctica.
Fundamento de la determinación de glucosa
Se realiza por el método de la glucosa oxidasa/peroxidasa, como valoración indirecta del peróxido de hidrógeno producido en la oxidación de glucosa catalizada por glucosa oxidasa:
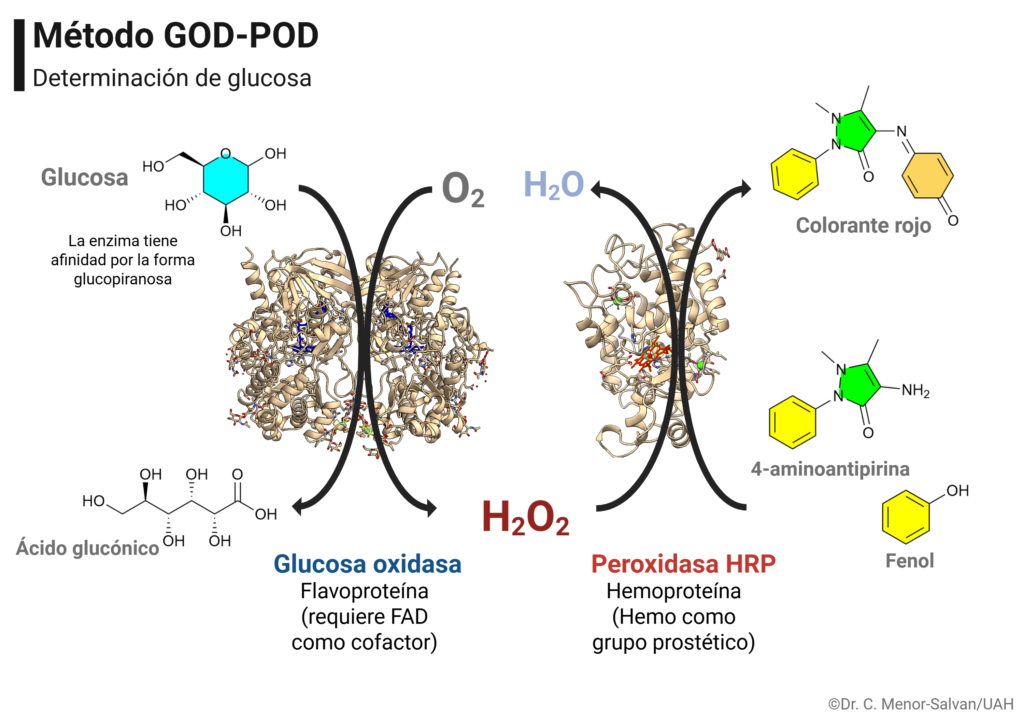
La formación de un color rojo/rosado es proporcional a la concentración de peróxido de hidrógeno, que es, a su vez, proporcional a la concentración de glucosa en la muestra. El método es muy sencillo de implementar y hay muchos kits comerciales.
Determinación colorimétrica
Para determinar la concentración de glucosa, primero hacemos un calibrado usando una solución de referencia de concentración conocida. Pero, a diferencia del método tradicional, que usamos en la práctica de determinación de proteínas por el método de Lowry, vamos a hacer la cuantificación usando un smartphone. Los datos que obtenemos son estos:

Se ve como, al aumentar la concentración de glucosa, aumenta la coloración roja. Hemos medido la absorbancia, como hacemos habitualmente, pero hay otros dos datos: G y B. ¿qué son?, ¿como los hemos obtenido?
En lugar de utilizar un espectrofotómetro, hemos utilizado el teléfono móvil con este sencillo montaje:

Un soporte para el móvil y la cubeta, hecho con una impresora 3D, y un fondo blanco (un papel o una pantalla blanca). Así, con el móvil vamos haciendo una foto de cada cubeta.
Después hemos usado la aplicación ‘Color Picker’. Al abrir cada imagen que hemos tomado (o midiendo directamente con la aplicación), obtenemos los valores RGB de cualquier punto de la imagen. El sistema RGB se basa en la idea de que podemos generar cualquier color mezclando diferentes proporciones de rojo (R), verde (G) y azul (B). Es el sistema estandard en pantallas digitales, y está directamente conectado con la absorbancia: si el color de la solución se va haciendo progresivamente más rojo, quiere decir que sus componentes complementarios, G y B, van a irse reduciendo. En especial uno de ellos. Lo que vemos es esto:
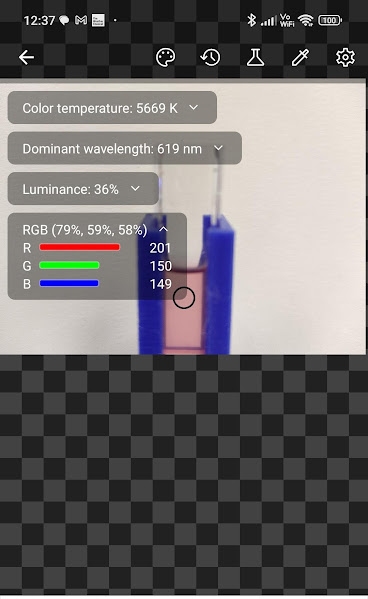
Como se ve, el código RGB de esta muestra es (201, 150, 149). Aquí es donde viene lo interesante. Esta es la relación entre el componente G y el color en nuestra recta de calibrado:
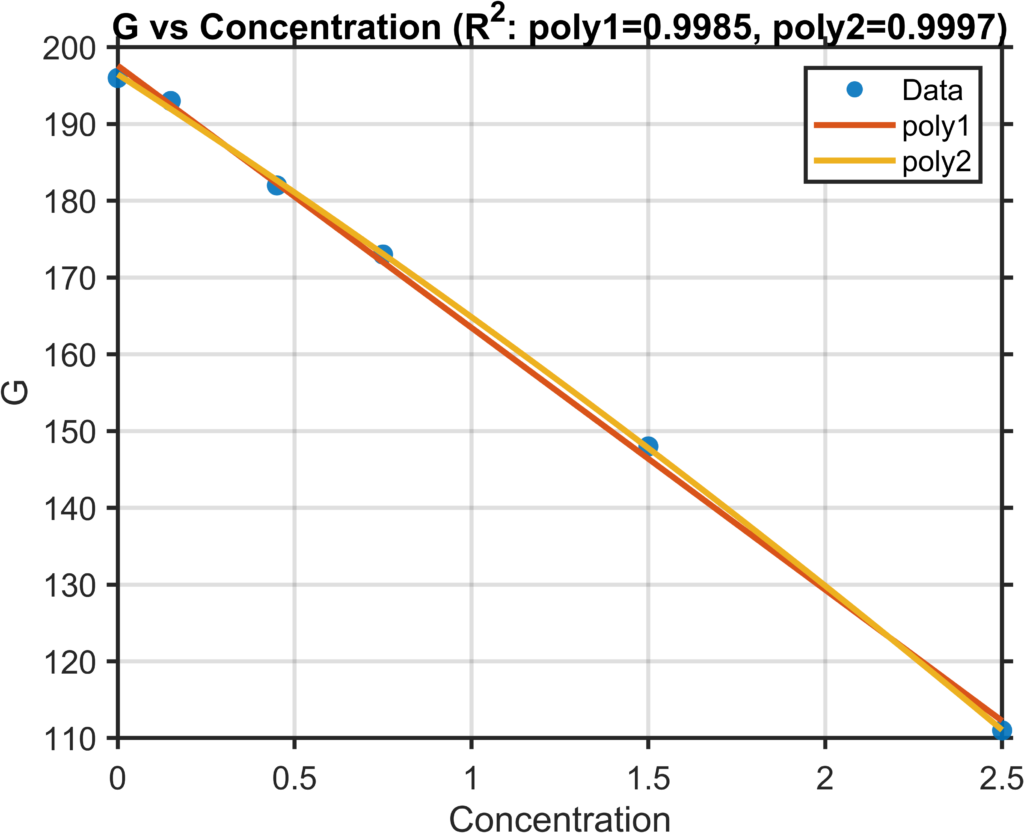
El ajuste es muy bueno. Tal como esperamos por la ley de Lambert-Beer, el ajuste es mejor a un polinomio de grado 2 (parábola), pero se puede aproximar a una recta en este rango de concentración. Lo curioso es que el ajuste es tan bueno o mejor que usando la absorbancia. En el caso de la componente B, el ajuste lineal empeora, la función es menos lineal, pero también funciona.
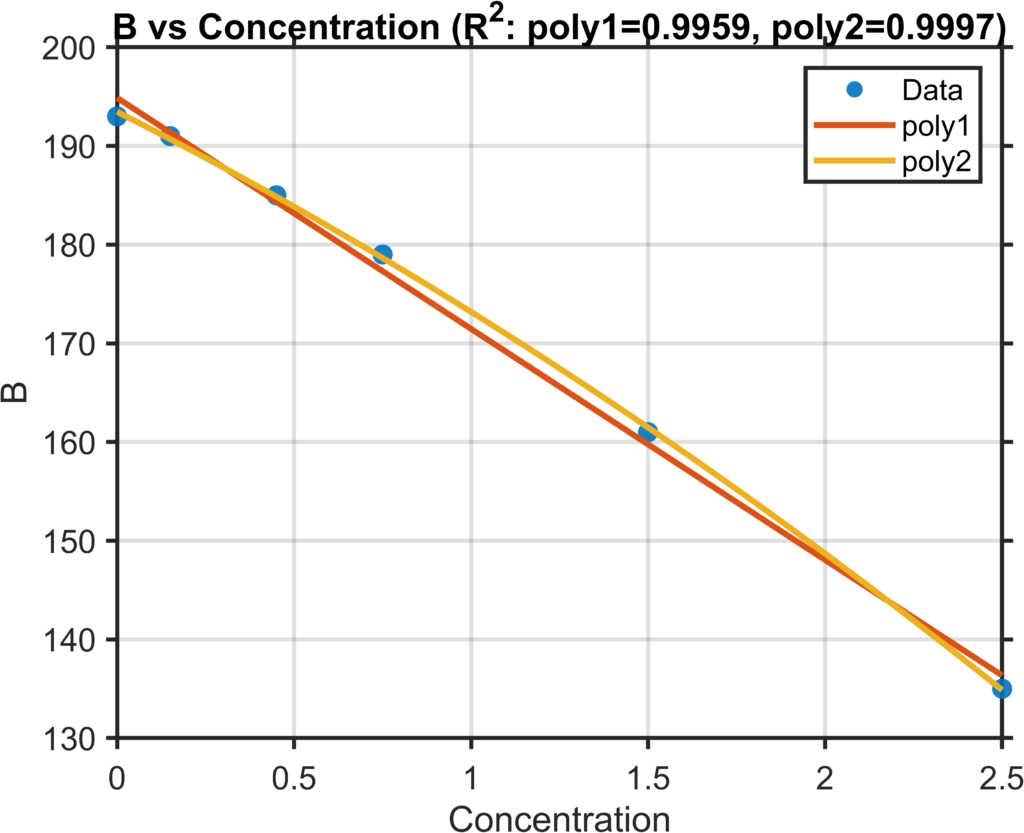
De hecho, al ser dos parámetros, podemos aprovecharlo y generar una función en 3D, en lugar de usar solo una de las rectas para interpolar los valores desconocidos:
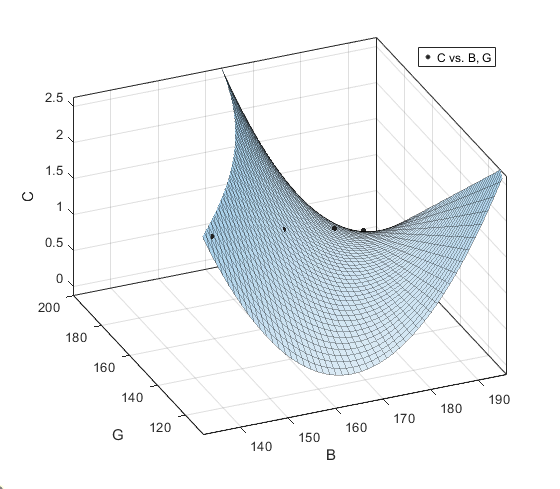
En este plano, si introduzco los valores de G y B medidos en una muestra desconocida, podré obtener la concentración correspondiente.
Analizando una muestra de concentración desconocida
Vamos a determinar la concentración correspondiente a la muestra del tubo 7 de la práctica (control):

Medimos con la aplicación Color Picker los parámetros RGB, y tenemos:
G = 177
B = 181
Interpolando en las rectas de calibrado, obtenemos las siguientes concentraciones:
C7 = 0.625 mg/dl (interpolación usando la relación concentración vs G);
C7 = 0.631 mg/dl (interpolando con la relación concentración vs B);
C7 = 0.610 mg/dl (interpolación combinada en 3D con G y B)
C7 = 0.614 mg/dl (interpolación usando absorbancias medidas con espectrofotómetro)
Como se ve la coincidencia de los diferentes métodos con el método típico de medida de absorbancias en espectrofotómetro da resultados bastante coherentes.
Cálculo de la concentración de glucógeno
Si seguimos el guión de la práctica, vemos que el tubo 7 se corresponde con el control diluído 1:10. Así que, si uso el valor de 0.610 mg/dl, tenemos que la concentración de glucosa en el tubo 7 es de 6.10 mg/dl.
La concentración en el tubo control, por tanto, es:
6.10 x 2000 µl / 70 µl = 174.3 mg/dl
El volumen total de la disolución analizada, resultante de la hidrólisis del glucógeno obtenido a partir de hígado, eran 5.4 ml. Por tanto, como 1 dl= 100 ml:
174.3 mg/ 100 ml x 5.4 ml = 9.412 mg de glucosa. Este es el contenido total de glucosa en la disolución control. Por tanto, 9.412 x 0.9 = 8.478 mg de glucógeno conseguimos aislar en el control.

Como la muestra original eran 0.5 g de hígado, esto implica que teníamos 16.9 mg de glucógeno por gramo de hígado. Si hubiera sido humano, como un hígado puede pesar entre 1.2 y 1.5 kg, ello implica que tendríamos alrededor de 20 gramos de glucógeno. La verdad es que es muy poco, pues un hígado tiene unos 80 a 100 g de glucógeno; un contenido de glucógeno tan bajo implica que podría llevar algún tiempo sin comer. O bien, que el análisis no ha sido muy bueno. Al fin y al cabo es una práctica.