ISOCITRATO DESHIDROGENASA, LA NUEVA ESPERANZA FRENTE AL CÁNCER
Redactado por Alba Cerrato Benítez, Laura Blanco García y María Ayala Molina. GRADO EN BIOLOGÍA SANITARIA, UAH
La isocitrato deshidrogenasa (IDH) es una enzima muy relacionada con el metabolismo de los carbohidratos. Esta enzima participa en la tercera reacción del ciclo de Krebs, catalizando el proceso de transformación del isocitrato en 2-oxoglutarato. Es la primera reacción de oxidación-reducción del ciclo en la que obtenemos poder reductor en forma de NADH. Esto hace que sea una importante proteína cuyas funciones explicaremos en el desarrollo de este trabajo.
La razón por la que escogimos esta enzima es por su importante papel en las dianas terapéuticas y en el desarrollo del cáncer. Recientes investigaciones han demostrado que la presencia de mutaciones en dos genes, IDH1 e IDH2 , se dan en los gliomas más comunes. Además, aunque no está muy claro si estas mutaciones están relacionadas con la esperanza de vida del paciente, existen estudios que apuntan a que las personas con estas alteraciones sobreviven durante más tiempo.
El estudio de este oncometabolito nos puede proporcionar información acerca del metabolismo de las células cancerosas y nos puede ayudar a descubrir nuevas líneas de investigación para el desarrollo de terapias contra el cáncer.
ESTRUCTURA
Actualmente, existen muchas isocitrato deshidrogenasas secuenciadas, sin embargo, el número de ellas con una estructura tridimensional resuelta está reducido. Concretando, solo encontramos las de los organismos Escherichia coli y Bacillus subtilis. Estas enzimas (IDH) catalizan la descarboxilación oxidativa del D-isocitrato, produciendo 2-oxoglutarato y CO2. Para ello es necesario NAD+ o NADP+ como coenzima y se produce NADH o NADPH, respectivamente.
Según su dependencia por la coenzima, podemos distinguir tres tipos fundamentales de IDH:
- IDH NAD+ – dependientes: necesitan como coenzima al NAD+ para catalizar la reacción. Aparece fundamentalmente en las mitocondrias de organismos del Dominio Eucarya. También hay organismos del Dominio Bacteria.
- IDH deshidrogenasas NADP+ -dependientes: requieren como coenzima al NADP+ para catalizar la reacción. Las encontramos en organismos de los tres Dominios: Eucarya, Bacteria y Archaea.
- IDH con especificidad dual: utilizan tanto el NAD+ como el NADP+ como coenzima. Este tipo es el único que aparece en arqueas termófilos y en algunas bacterias.
En los seres humanos, existen tres isoformas de esta enzima:
- IDH3 dependiente de NAD+, cataliza uno de los pasos del ciclo de Krebs en la mitocondria. Es necesaria para la respiración celular.
- IDH1 y IDH2 son dependientes de NADP+, y por lo tanto aportan poder reductor a la célula en forma de NADPH. Se localizan en el citosol, y también en la mitocondria y el peroxisoma.
En el desarrollo de este trabajo nos centraremos en la estructura de la IDH1.
La IDH1 es una proteína α/β, es decir, la estructura de esta proteína está constituida por la alternancia de láminas beta y hélices alfa, cuyo núcleo es hidrófobo. Puede formar un dímero de dos subunidades iguales o un tetrámero formado por dos dímeros, este último parece ser la forma funcional de la proteína.
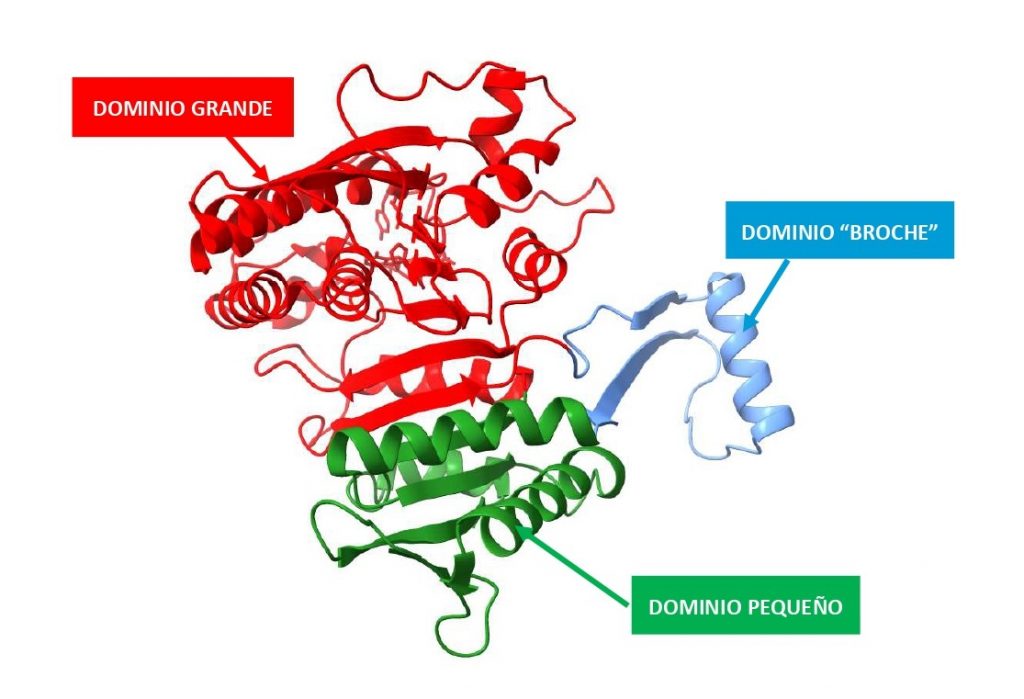
Podemos distinguir en cada subunidad 3 dominios: dominio grande, dominio pequeño y dominio “broche”. La dimerización y tetramerización que hemos mencionado anteriormente está mediada por interacciones a nivel de los dominios “broche” y de los dominios pequeños.

Encontramos una lámina β que une los dominios grande y pequeño, y que además a ambos lados presenta dos surcos de naturaleza hidrofílica. En el surco formado por los dominios grande y pequeño de una subunidad y por el dominio pequeño de la subunidad adyacente encontramos el centro activo. Existen 2 sitios activos por cada dímero proteico.
PAPEL BIOLÓGICO
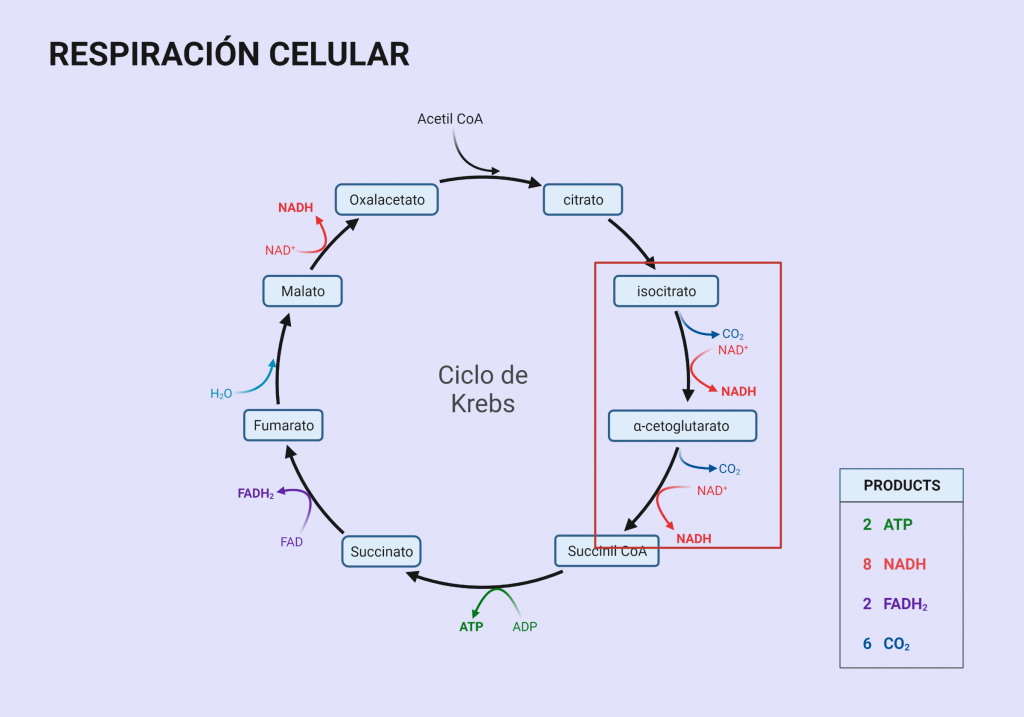
Las isocitrato deshidrogenasas son una familia de enzimas que catalizan la reacción de descarboxilación oxidativa de isocitrato en α-cetoglutarato (o 2-oxoglutarato) en el ciclo de Krebs. La regulación de la actividad enzimática de la isocitrato deshidrogenasa es muy importante para llevar a cabo las funciones biológicas. Estas enzimas tienen dos cofactores distintos: NAD+ y NADP+. En el caso de la IDH1, isoenzima en la que nos hemos centrado, el cofactor es el NADP+ (que utiliza como aceptor de electrones) y se encuentra principalmente en el citoplasma. Por lo tanto, otra de sus funciones será reducir NADP+ a NADPH. En el proceso de esta reacción se libera uno de los átomos de carbono del reactivo en forma de dióxido de carbono (CO2) y dos átomos de hidrógeno, uno de los cuales se transfiere al transportador (NADP+), que lo utilizará para impulsar la rotación de la ATP sintetasa. La reacción que la enzima lleva a cabo en el ciclo de Krebs cuenta con un intermedio de reacción que es el oxalosuccinato.
Además del papel catabólico que tiene la enzima en el ciclo de Krebs, se ha demostrado que tienen una función importante en la defensa de la célula contra el daño oxidativo a través de la generación de NADPH. Asimismo, la IDH citosólica contiene una secuencia de direccionamiento peroxisomal de tipo 1 que se encarga de dirigir diferentes proteínas hacia los peroxisomas. También se han encontrado isocitrato deshidrogenasas citosólicas (IDH1) en peroxisomas de levaduras y de células hepáticas humanas y de rata y se ha podido demostrar que son necesarias para la β-oxidación de ácidos grasos insaturados. Su función en la β-oxidación es provisionar con NADPH a los peroxisomas.
En algunas células bacterianas solo existe un tipo de isocitrato deshidrogenasa (IDH) dependiente de NADP+, cuyas funciones y estructuras también han sido estudiadas. En el caso de estos organismos, la enzima actúa en un punto muy importante entre el ciclo de Krebs y el ciclo de glioxilato. Mediante la regulación de su actividad, se puede regular la cantidad de sustrato de las dos reacciones. La fosforilación de un aminoácido de Serina (Ser) que se sitúa en el sitio de unión al que se une el ion isocitrato-metal, la actividad de la IDH de las bacterias es regulada. Sin embargo, el mecanismo regulador que controla la IDH1 en mamíferos no está claro. Aunque las enzimas en mamíferos y en bacterias se parecen, tan solo comparten el 20% de similitud en su secuencia. Sin embargo, la secuencia de la IDH en mamíferos tiene una Serina en la posición equivalente a la que poseen las bacterias en su secuencia. Esto sugiere que las IDH1 de mamíferos también puedan tener un sitio de unión que pueda ser fosforilado.
MECANISMO DE ACCIÓN
Las diferentes conformaciones que adopta el complejo enzimático provocan cambios en la
estructura del centro activo. Podemos observar:
- Conformación abierta (inactiva): Si no hay isocitrato, el surco del centro activo está abierto y
el surco posterior cerrado. La interacción entre el Asp279 del dominio pequeño con la Ser94
del dominio grande estabiliza la estructura y, además, en la zona donde se encuentra el
Asp279 encontramos una estructura extendida. Esa interacción impide la unión del isocitrato. - Conformación cerrada (activa): Si la concentración del isocitrato y del catión divalente llega a un cierto nivel, se une al centro activo. Rompiendo la interacción (puentes de hidrógeno) entre el Asp279 y Ser94, produciéndose la expulsión del Asp279 y la interacción con el Ca2+. La estructura extendida que se encontraba en la zona donde se encontraba, adopta una
estructura en hélice α. Esto permite la entrada del isocitrato. Se cierra el centro activo y se
abre el surco posterior.
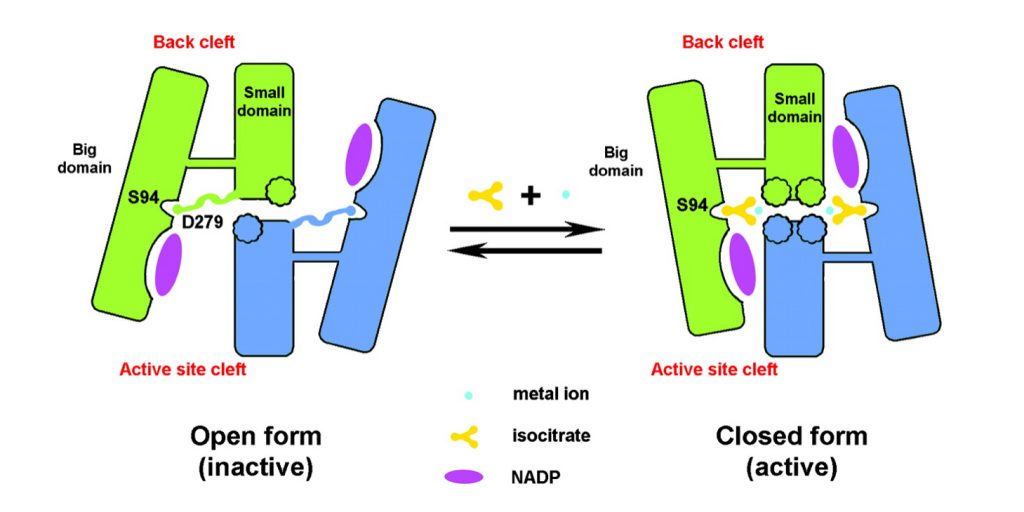
Este cambio conformacional que se produce entre la forma activa e inactiva se debe a un movimiento de bisagra de las láminas β que se encuentra entre el dominio «broche» y el dominio pequeño.
IMPORTANCIA BIOMÉDICA: UNA ESPERANZA PARA EL CÁNCER
Los gliomas son los tumores primarios más comunes del sistema nervioso central, por lo que afectan a las funciones del corazón y la médula espinal. Según la Organización Mundial de la Salud, los gliomas se clasifican de I a IV según su grado de malignidad. Recientemente, se ha descubierto una posible relación de la aparición de los mismos con las mutaciones en el exón 4 de los genes que codifican las isocitratos deshidrogenasas 1 y 2. En el caso de la isocitrato deshidrogenasa 1, con los gliomas de grado II-III o la leucemia mieloide aguda entre otros.
El gen IDH1 se encuentra localizado en 2q33.3 y su ARNm contiene 10 exones para codificar la isocitrato deshidrogenasa 1 (414 aminoácidos). En relación con las mutaciones, nos interesa especialmente el residuo 132 de la proteína, correspondiente a una arginina altamente conservada en todas las isoformas de la enzima, que va a sufrir cambios a distintos aminoácidos.
| Cambio de aminoácido | N (%) |
| R132H | 92,7 |
| R132C | 3,6 |
| R132S | 1,8 |
| R132G | 0,9 |
| R132L | 0,5 |
| R132V | 0,5 |
Como hemos observado, la mutación más frecuente es la que cambia una arginina por una histidina (R132H). Pero, ¿Qué consecuencias lleva asociadas dicha mutación? ¿Tanta importancia tiene el cambio de un único aminoácido?
Como se ha mencionado con anterioridad, la isocitrato deshidrogenasa salvaje (no mutante), está involucrada en la descarboxilación oxidativa del isocitrato a 2-oxoglutarato y dióxido de carbono con la reducción de NADP+ a NADPH. El NADPH obtenido se utiliza para la producción de glutatión reducido, un tripéptido encargado de neutralizar los radicales libres, toxinas y oxidantes que se generan en las células, favoreciendo la supervivencia celular y la anti-apoptosis.
Sin embargo, lo que ocurre al cambiar un aminoácido (arginina) del sitio activo de la enzima por otro (histidina) es que la enzima pierde su capacidad de catalizar la conversión de isocitrato a 2-oxoglutarato. En su lugar, la enzima adquiere la capacidad de catalizar la reducción dependiente del NADPH del 2-oxoglutarato a 2-hidroxiglutarato. Una de las consecuencias de la producción excesiva del oncometabolito, 2-hidroxiglutarato, es la formación e incremento de la malignidad de gliomas.
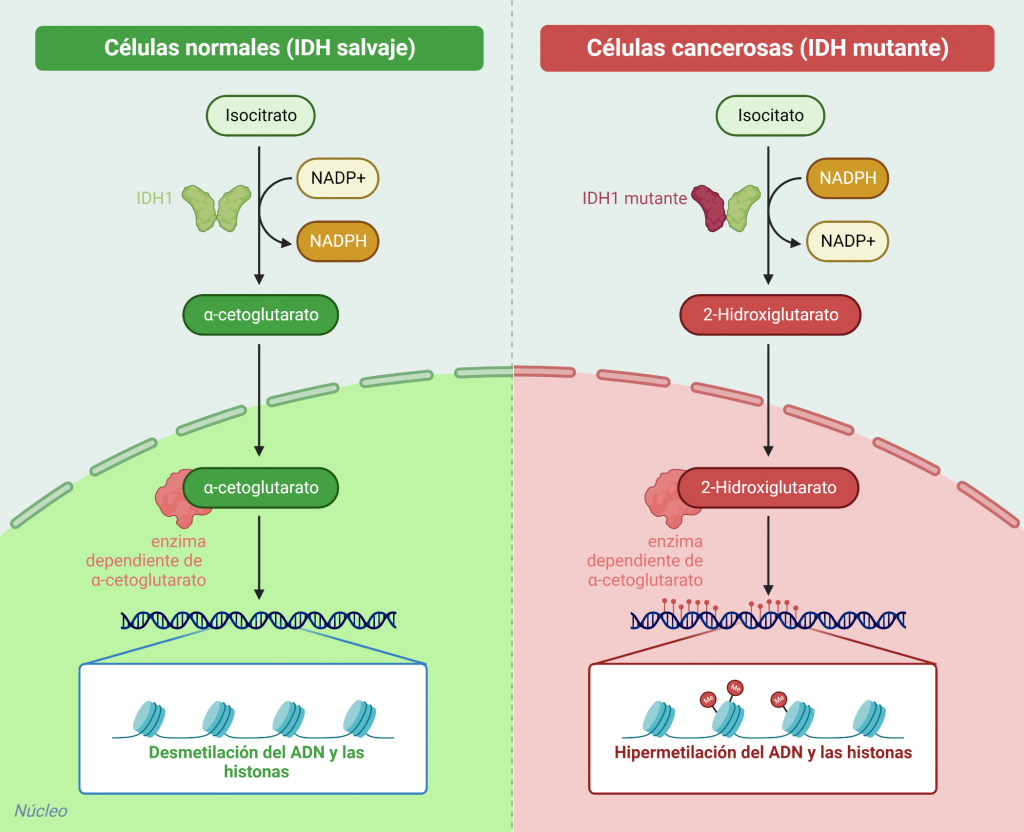
Además, el 2-hidroxiglutarato, al ser tan parecido en estructura al 2-oxoglutarato, funciona como un inhibidor de las enzimas dependientes de 2-oxoglutarato. Estas enzimas tienen un papel muy importante en el mantenimiento del equilibrio de las histonas y la metilación del ADN por lo que, un exceso de 2-hidroxiglutarato podría causar la hipermetilación de histonas y ADN y el bloqueo de la diferenciación celular.
Diversos estudios indican que la probabilidad de que un paciente que presenta dicha mutación se recupere, es mayor que la de un paciente que no la presenta en el caso de gliomas de bajo grado. Para el resto de gliomas, la situación varía: en algunas ocasiones resulta en un valor de pronóstico desfavorable y, en otras, aún no se ha encontrado relación. Además, ha resultado ser una herramienta útil para diferenciar los gliomas de otras lesiones benignas y diferenciar entre gliomas primarios y secundarios.
Estos descubrimientos han abierto un nuevo campo de investigación e innovación farmacológica: la búsqueda de inhibidores de las IDH mutantes.
REFERENCIAS / BIBLIOGRAFÍA
Balss, J., Meyer, J., Mueller, W., Korshunov, A., Hartmann, C. y von Deimling, A. (2008). Análisis de la mutación del codón 132 de IDH1 en tumores cerebrales. Acta neuropathologica , 116 , 597-602.
Dang, L., White, D. W., Gross, S., Bennett, B. D., Bittinger, M. A., Driggers, E. M., Fantin, V. R., Jang, H. G., Jin, S., Keenan, M. C., Marks, K. M., Prins, R. M., Ward, P. S., Yen, K. E., Liau, L. M., Rabinowitz, J. D., Cantley, L. C., Thompson, C. B., Heiden, M. G. V., & Su, S. M. (2009). Cancer-associated IDH1 mutations produce 2-hydroxyglutarate. Nature, 462(7274), 739-44. https://doi.org/10.1038/nature08617
Etxaniz Ulazia, O. (2017). Investigación de las mutaciones de los genes de IDH1 y 2 en los gliomas de bajo grado [Tesis doctoral]. Universidad Autónoma de Barcelona.
García Martínez, A. (2016). Estudio de biomarcadores en gliomas y su utilidad clínica [Tesis doctoral]. Universidad de Alicante.
PDB101: Molecule of the Month: Isocitrate Dehydrogenase. (s. f.). RCSB: PDB-101. https://pdb101.rcsb.org/motm/129
Liu, Z., Yao, Y., Kogiso, M., Zheng, B., Deng, L., Qiu, J. J., Dong, S., Lv, H., Gallo, J. M., Li, X. N., & Song, Y. (2014). Inhibition of Cancer-Associated Mutant Isocitrate Dehydrogenases: Synthesis, Structure–Activity Relationship, and Selective Antitumor Activity. Journal of Medicinal Chemistry, 57(20), 8307-8318. https://doi.org/10.1021/jm500660f
¿Qué es el Glutatión Reducido y para qué sirve? (s. f.). https://www.tarracofarma.com/que-es-el-glutation-reducido-y-para-que-sirve
Reitman, Z. J., & Yan, H. (2010). Isocitrate Dehydrogenase 1 and 2 Mutations in Cancer: Alterations at a Crossroads of Cellular Metabolism. JNCI Journal of the National Cancer Institute, 102(13), 932-941. https://doi.org/10.1093/jnci/djq187
Ricaurte O, Neita K, Valero D, Ortega-Rojas J, Arboleda-Bustos CE, Zubieta C, Penagos J, Arboleda G. Estudio de mutaciones en los genes IDH1 e IDH2 en una muestra de gliomas de población colombiana. biomedica [Internet]. 1 de mayo de 2018 [citado 1 de febrero de 2023];38(Sup1):86-92. Disponible en: https://revistabiomedica.org/index.php/biomedica/article/view/3708
Robert, T. (s. f.-c). Dpto. Bioquímica y Biología Molecular. http://proteinasestructurafuncion.usal.es/moleculas/IsocitratoDeshidrogenasas/index.html
Sumihito Nobusawa, Takuya Watanabe, Paul Kleihues, Hiroko Ohgaki; Mutaciones de IDH1 como firma molecular y factor predictivo de glioblastomas secundarios. Clin Cancer Res 1 de octubre de 2009; 15 (19): 6002–6007. https://doi.org/10.1158/1078-0432.CCR-09-0715
UCSF ChimeraX: Structure visualization for researchers, educators, and developers. Pettersen EF, Goddard TD, Huang CC, Meng EC, Couch GS, Croll TI, Morris JH, Ferrin TE. Protein Sci. 2021 Jan;30(1):70-82.
Vista de Estudio de mutaciones en los genes IDH1 e IDH2 en una muestra de gliomas de población colombiana. (s. f.-b). https://revistabiomedica.org/index.php/biomedica/article/view/3708/3915
Xu, X., Zhao, J., Xu, Z., Peng, B., Huang, Q., Arnold, E. y Ding, J. (2004). Las estructuras de la isocitrato deshidrogenasa dependiente de NADP citosólica humana revelan un nuevo mecanismo de autorregulación de la actividad. Revista de química biológica , 279 (32), 33946-33957.
Zachary J. Reitman, Hai Yan, Isocitrate Dehydrogenase 1 and 2 Mutations in Cancer: Alterations at a Crossroads of Cellular Metabolism, JNCI: Revista del Instituto Nacional del Cáncer , volumen 102, número 13, 7 de julio de 2010, páginas 932–941, https ://doi.org/10.1093/jnci/djq187