Mecanismo de actuación de los alcaloides de la vinca como antitumorales
Ignacio Moratilla Rivera. Biología Sanitaria-Universidad de Alcalá de Henares.
La vincapervinca (Vinca minor) y la vinca de Madagascar (Catharanthus roseus) son plantas de la familia de las apocináceas que destacan por su gran belleza. Es bastante común encontrarlas en jardines como ornamentales (por ejemplo, en los jardines colgantes de Madrid) y también son de hábito silvestre. Pero a pesar de su anodina apariencia contiene una serie de compuestos químicos que tienen la capacidad de luchar contra el cáncer.
Estos compuestos son los conocidos como alcaloides de la vinca. Tenemos dos muy conocidos pero existen muchos más, estos son la vinblastina y la vincristina. Algunos se han creado sintéticamente como la vinflunina.
Los alcaloides de la vinca fueron los primeros alcaloides biosintetizados en plantas que se usaron para remediar el cáncer.
Su mecanismo de acción consiste en la inhibición de la polimerización de los microtúbulos, que como sabemos son imprescindibles para llevar a cabo la división celular. Las células cancerosas se caracterizan por su inusitada capacidad proliferativa, por lo que la propiedad de estos alcaloides los hace idóneos para frenar su avance.
BOTÁNICA
Tanto la V. minor como C. roseus pertenecen a la familia Apocynaceae, al igual que la adelfa (Nerium oleander), Rauvolfia serpentaria o el estrofanto (Strophantus).
V. minor suele ser rastrera o puede trepar sobre tutores. Esta presenta hojas pediculadas, elípticas y opuestas, normalmente de un color verde oscuro. Las flores suelen ser lilas con cinco pétalos soldados en la base, dando las partes libres un aspecto de hélice. El centro de las flores encontramos un hueco cuyos bordes delimitan una estrella y en su interior se hallan los órganos reproductores.
C. roseus es muy similar a la vinca, aunque teniendo las hojas menos puntiagudas. Lo más característico y bello son las flores. Estas oscilan en una gran gama cromática de rosas, rojas, magentas y blancos. Presentan 5 pétalos y el centro de la flor presenta un agujero circular que alberga el androceo y gineceo.

Ambas son especies monoicas de flores hermafroditas.
MICROTÚBULOS
Los microtúbulos son estructuras tubulares que forman parte del citoesqueleto y van a intervenir en diversas funciones como dar forma a la célula, transporte, transducción de señales y, lo más relevante ahora, el movimiento de los cromosmas.
Están constituidos por dos proteínas globulares que se organizan en espiral: son la tubulina α y la tubulina β.
Estas estructuras no son siempre estables como en axones neuronales o cilios, sino que pueden estar en constante polimerización y despolimerización.
Para la polimerización las tubulinas se incorporan en dímeros de β y α tubulina, los cuales previamente se han debido de unir con GTP. Los dímeros se unen por uno de los extremos del microtúbulos, y pasado un tiempo el GTP de la tubulina β se hidroliza al GDP, mientras que el de la tubulina α no lo hace.
La unión del GTP no es covalente, sino que se estabiliza por puentes de hidrógeno de grupos OH y NH2 de las cadenas laterales de los aminoácidos presentes en el sitio de unión. Además existe un átomo de Mg2+ que estabiliza su posición. Por último, la base de guanina forma un stacking con un residuo de Tyr.
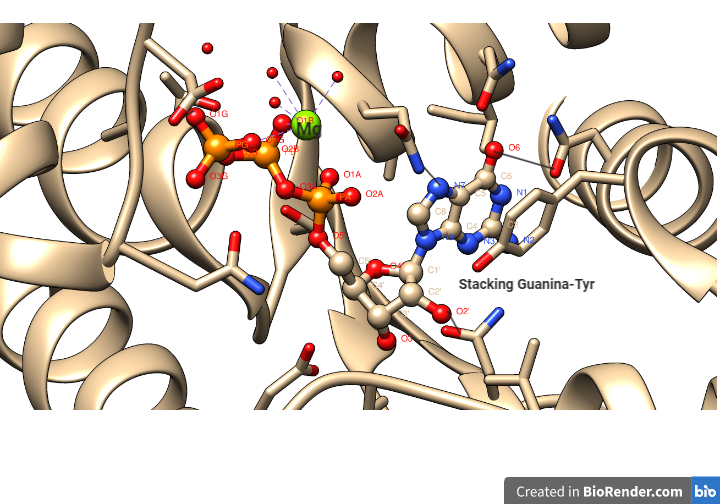
Dicha unión previa a GTP debe ser correcta para el óptimo ensamblaje de los microtúbulos.
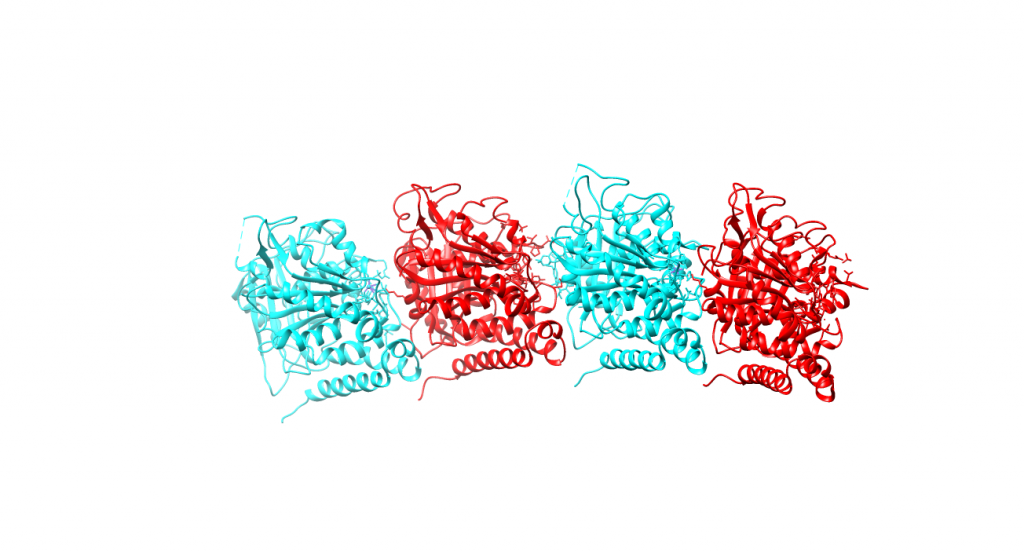
Vinblastina y vincristina
Estas dos moléculas son sintetizadas a partir de otros dos alcaloides indólicos (derivados del Trp), esto hace que tengan es su estructura dos grupos indol (heterociclo nitrogenado) y se conozcan como alcaloides binarios. Son acumuladas en las partes aéreas de las plantas y en bajas concentraciones.
-
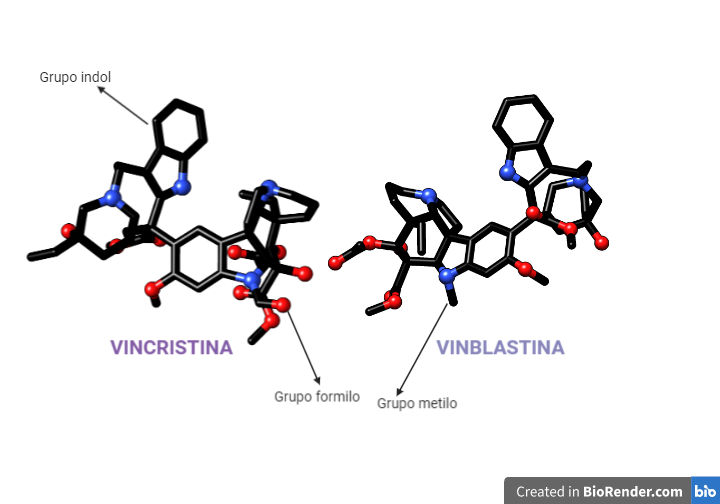
Figura 3: Imagen realizada con Chimera y BioRender. Pone de manifiesto las diferencias y semejanzas entre vinblastina (PDB: 1Z2B) y vincristina (PDB: 7A69)
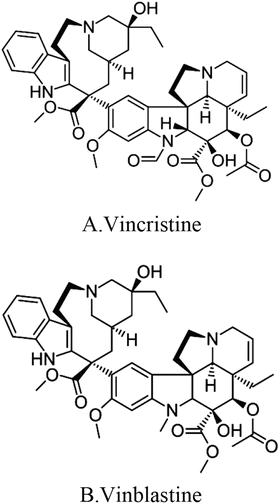
Estas dos se diferencian la una de la otra en un solo radical: la viblastina tiene grupo metilo y la vincristina tiene grupo formilo. Este sutil cambio hace que sus propiedades anticancerígenas cambien. Los dos no afecta por igual a todos los tipos de neoplasias.
La vinblastina ha sido empleada en linfomas de Hodgking, cáncer de células germinales en el testículo y cáncer de mama.
La vincristina se ha utilizado en leucemias, linfomas y neuroblastomas.
Vamos a centrarnos en el mecanismo molecular de la inhibición de la polimerización.
La tubulina β presenta en su estructura el conocido como domino de unión a vinca. Es en esta región donde se unen estos alcaloides.
Esta zona se encuentra adyacente al sitio de unión de GTP de la tubulina, produciendo un cambio conformacional que impide la correcta unión del nucleótido y que por lo tanto no pueda realizarse satisfactoriamente la polimerización de los microtúbulos.
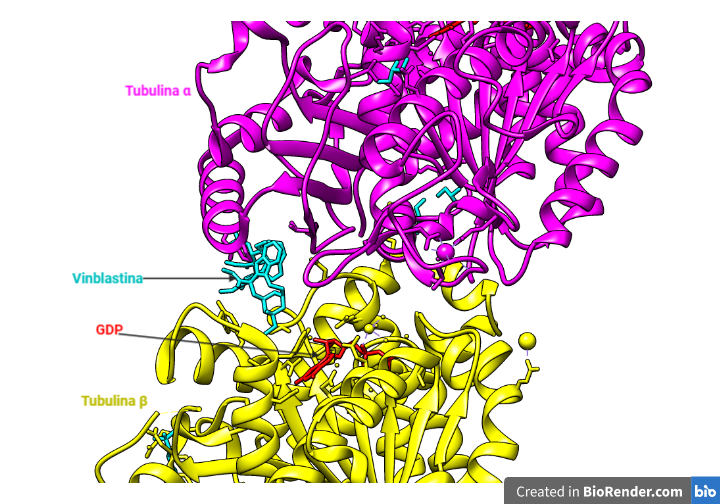
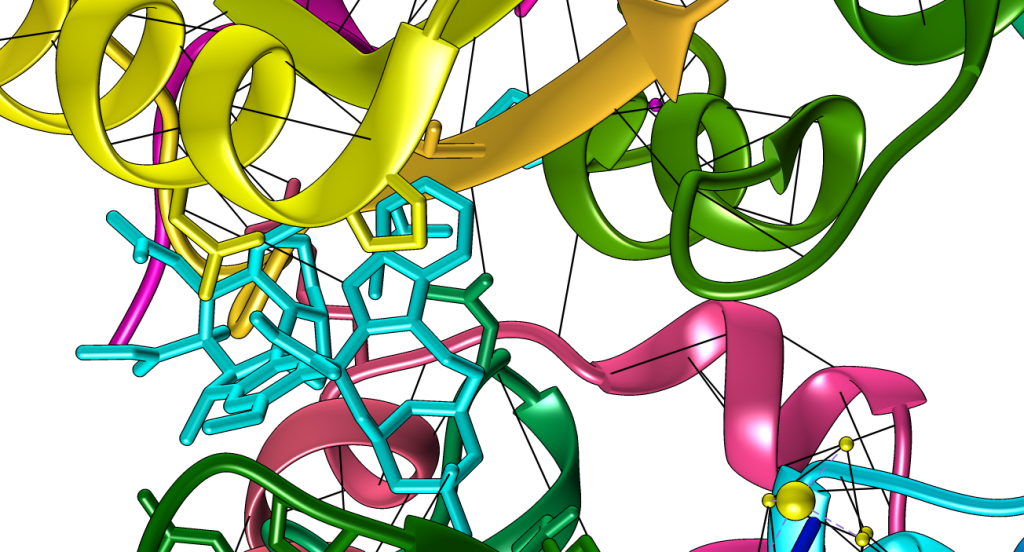
La unión tiene una alta afinidad y es reversible, producida por puentes de hidrógeno. Estos son dos en la vinblastina establecidos por una Asn con N del grupo indol y un oxígeno que forma parte de un enlace peptídico con un grupo OH.
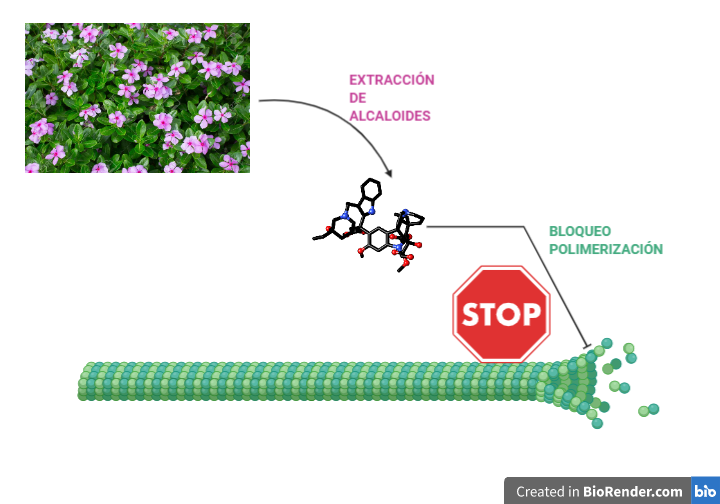
En las divisiones celulares los microtúbulos están en constante polimerización y despolimerización, ya que tienen que colocar los cromosomas en el ecuador de la célula formando la placa metafásica o plano ecuatorial. De tal manera que los alcaloides detienen la división justo en el momento de la metafase.
TOXICIDAD
Una vez entendido cómo actúan estos compuestos no es de extrañar que traigan consigo una serie de efectos secundarios tóxicos para el paciente. Se pueden intentar paliar mediante una disminución en la frecuencia de la toma o bajando la dosis.
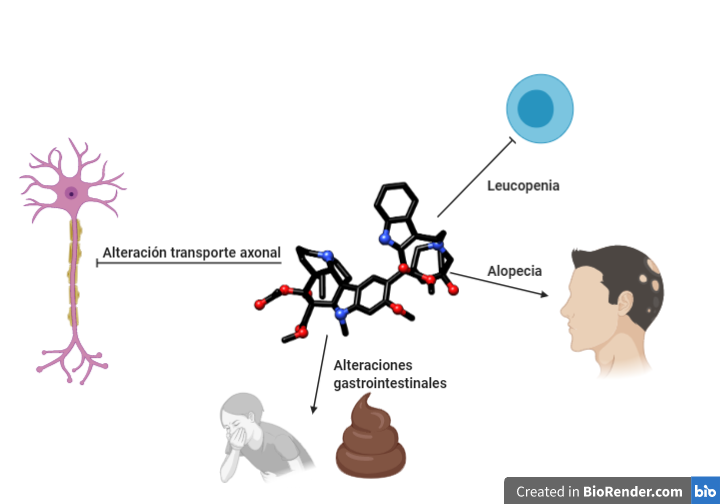
La neurotoxicidad es común en estos alcaloides, pero parece que es más severa la vincristina. Las neuronas realizan el transporte axonal a través de microtúbulos y proteínas como la quinesina y la dineina. Al interferir en el ensamblaje de estos componentes citoesqueléticos la células nerviosas disminuyen su transporte generando problemas a nivel del sistema nervioso central (alucinaciones, confusión, insomnio o depresión) y periférico (hormigueo, dolor muscular).
Otras afecciones comunes son las gastrointestinales debido a lo prolíficas que son las células epiteliales del intestino, cursando con dolor abdominal, nauseas, diarrea o estreñimiento. Por este mismo motivo también se produce la caída del cabello o alopecia.
Se han reportado también casos de azoospermia, ceguera, disnea y broncoespasmo.
Debido al efecto leucopenizante de la vinblastina, durante la medicación se debe evitar la vacunación por su posible reactividad. Se contraindica además para mujeres embarazas como para aquellas que estén proporcionando lactancia.
Referencias:
1. Moudi M, Go R, Yien CY, Nazre M. Vinca alkaloids. Int J Prev Med. 2013;4(11):1231-1235.
2. Grindey, G. B. (1989) ‘Vinca alkaloids.’, Current opinion in oncology, 1(2), pp. 203–205. doi: 10.1016/B978-0-444-53717-1.01632-2.
3. Paniagua R, Nistal M, Sesma P, Álvarez-Uría M, Fraile B, Andón R, Sáez F.J. (2007). Biología celular y molecular 4ª edición. Madrid. Ed: Mc Graw Hill Education.
4. Bruneton J. (2001). Farmacognosia, fitoquímica, plantas medicinales 2ª edición. Ed: Acribia.