Por Lorena Pérez Fernández y Elena Quintas Rubio, Biología Sanitaria, UAH
Introducción
La bomba de sodio potasio es una proteína perteneciente a la familia de las ATPasas de tipo P. Este tipo de ATPasas se encuentra en la membrana plasmática de las células y funciona mediante un impulso de iones usando energía en forma de ATP. Esta bomba, en concreto, establece gradientes de concentración de iones de sodio y de potasio a través de la membrana plasmática en todas las células animales, al bombear sodio desde el citoplasma y potasio desde el medio extracelular.
Esta bomba participa en el impulso nervioso, muy necesario para el funcionamiento correcto del organismo. Por ello, la bomba requiere de mucha energía, llegando a usar hasta un tercio del ATP que producen nuestros cuerpos.
Función biológica y mecanismo de la proteína
El sistema de bomba de sodio-potasio mueve iones de sodio y potasio en contra de grandes gradientes de concentración. Mueve dos iones de potasio en la célula, donde los niveles de potasio son altos y bombea tres iones de sodio fuera de la célula en el líquido extracelular. Este movimiento de iones es en contra de gradiente electroquímico, por lo requiere de ATP.
La bomba de sodio-potasio se encuentra en la membrana plasmática de casi todas las células humanas y es común en toda la vida celular. Ayuda a mantener el potencial de células y regula el volumen celular.
La célula introduce sodio a través del cotransportador de sodio-glucosa. A la vez que se introduce glucosa, el sodio entra también sirviendo de impulso.
La célula debe restaurar los niveles de sodio sacando sodio. Para ello es necesario la acción de la bomba sodio-potasio, que saca tres iones de sodio a la vez que introduce dos de potasio. Inicialmente, la célula ha sacado potasio para bajar su concentración plasmática y que la bomba realice su correcto funcionamiento.
En condiciones habituales, la célula tiene un exceso de potasio y cierto déficit de sodio respecto al medio. La bomba se encarga de mantener dichos niveles.
Este movimiento de iones en contra de gradiente genera un exceso de carga negativa en el interior de la célula y un exceso de carga positiva en el exterior.
Esta diferencia en las cargas provoca voltaje a través de la membrana. El voltaje es la energía potencial eléctrica que es causada por una separación de cargas opuestas, en este caso a través de la membrana. El voltaje a través de una membrana se denomina potencial de membrana, el cual es muy importante para la conducción de impulsos eléctricos a lo largo de las células nerviosas.
La función principal de la bomba sodio/potasio es mantener estable la concentración de iones de sodio y potasio en sus niveles requeridos a ambos lados de la membrana para que se establezca correctamente el potencial de membrana y puedan transmitirse los impulsos nerviosos.
Estructura
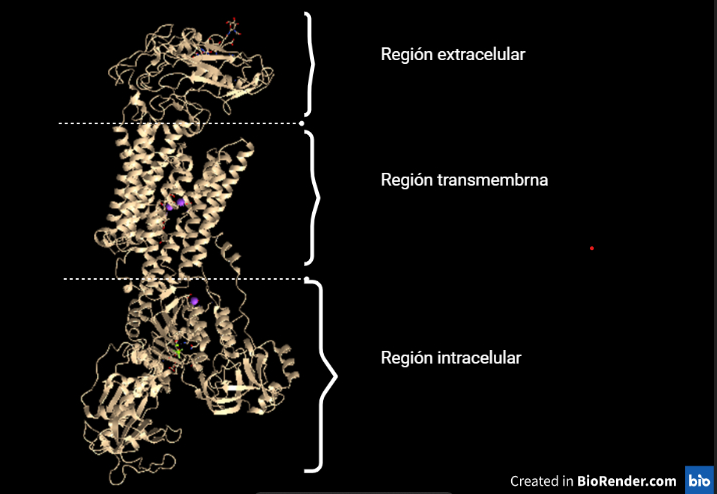
Estructuralmente, la bomba se compone de una subunidad catalítica alfa y una subunidad auxiliar beta, es decir, es indispensable para el funcionamiento de la bomba, pero no participa directamente en su actividad. La subunidad alfa contiene una región transmembrana compuesta por 10 hélices. Entre estas hélices, se encuentran los sitios de unión de la molécula de ATP y los iones de sodio y potasio, que son varios. Hay tres sitios de unión que unen el sodio en el estado E1 y dos sitios que unen el potasio en el estado E2. El estado E1 es aquel en el que la bomba está orientada hacia el interior de la célula para captar tres iones de sodio que van a ser expulsados. El estado E2 es aquel en el que la bomba está orientada hacia el medio extracelular para captar dos iones de potasio que van a ser introducidos en la célula.

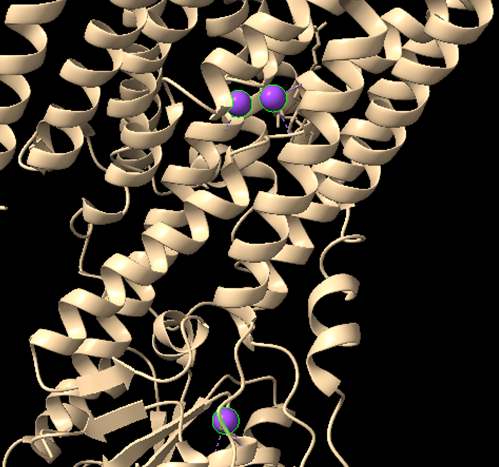
Las esferas moradas de la imagen representan iones de potasio unidos a la molécula. La esfera que se encuentra en la región intracelular (parte de abajo) adquiere cierta importancia, ya que está implicada en la activación de la desfosforilación, proceso requerido para el cambio de estado de la bomba de E1 a E2.
Los dos iones más próximos presentan distintas coordinaciones y uniones respecto al ion solitario. La unión de estos iones establece el estado E2, el cual, presenta menor afinidad por el sodio. Esto se debe a las distintas interacciones que cada ion del par establece con las estructuras de su alrededor.
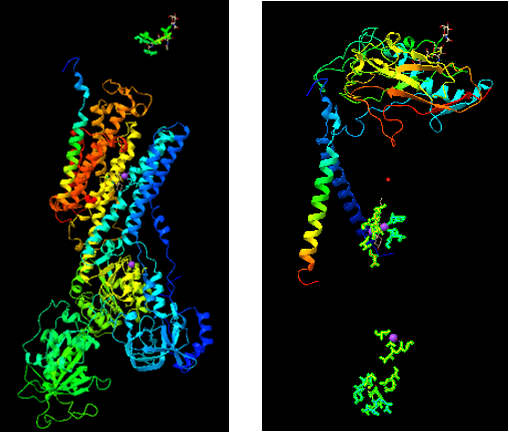
En concreto, la proteína enzimática está conformada por dos subunidades proteicas de tipo alfa (α) y dos de tipo beta (β). Se trata de un tetrámero (α2β2), cuyas proteínas integrales atraviesan la bicapa lipídica que forma las membranas de las células.
Ambos tipos de subunidades presentan variaciones llegando a encontrar tres isoformas para la subunidad alfa (α1, α2 y α3) y tres para la beta (β1, β2 y β3).
Las subunidades alfa contiene los sitios de unión para la molécula de ATP y los iones de sodio y potasio. Al ejercer la función de la bomba, forman el componente catalítico de la enzima. Las diferentes isoformas se pueden encontrar en diversos tejidos tales como el muscular, el adiposo o el cerebral.
Las subunidades beta no participan de forma directa en la función catalítica de la bomba, pero sí poseen gran importancia para el buen funcionamiento de la bomba. Ayudan en la estabilización y en la señalización. Además, cualquier cambio o mutación en estas subunidades pueden afectar la unión de los iones y las propiedades de la proteína. Se tratan de glicoproteínas con un solo dominio transmembrana, aunque varios de los residuos glucídicos se pueden observar en región extracelular.
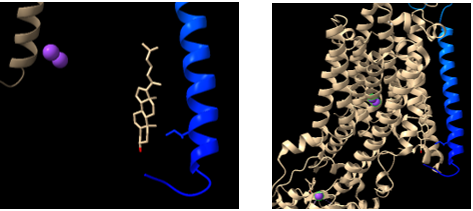
La hélice en la región transmembrana se encuentra ligeramente separada de la región alfa, presentando distinta inclinación en relación con las demás hélices. El contacto con dos hélices transmembrana de la subunidad alfa se consigue principalmente a través de dos grupos de residuos aromáticos. La combinación de los distintos residuos que forman los anillos se forma con ambas subunidades. Se encuentran altamente coordinados y cualquier mutación podría causar una alteración en la afinidad de unión al potasio.
Implicaciones biomédicas
Como se ha mencionado anteriormente, la bomba de sodio potasio se encarga de mantener las concentraciones de ambos iones estables, por lo que cuando esto no se cumple, se da lugar a patologías como la hipertensión arterial.
Ante la ingesta de un exceso de sodio, este es absorbido rápidamente por el intestino aumentando la concentración molar, lo cual hace que el individuo tenga sensación de sed. Por la ingesta de agua se expande el volumen intravascular. Para compensar esto, los riñones se encargan de eliminar el exceso de sodio y agua. Se considera la hipertensión arterial como un mecanismo necesario para aumentar la excreción renal de sodio. Es decir, ante un defecto patológico que impidiera la eliminación del sodio, la presión arterial debe aumentar; de esta manera aumenta la presión de filtración en los glomérulos que incrementaría la excreción urinaria de sodio. Habitualmente existe un balance, pero ante un consumo excesivo de sodio aparecería la hipertensión.
El aumento de sodio en el medio extracelular hace que se estimule la actividad de la bomba sodio/potasio. Sin embargo, se puede inhibir en presencia de sustancias digitálicas, cuya síntesis y secreción se ve estimulada por el exceso de sodio. La bomba tiene capacidad de unirse a una sustancia de efecto digitálico (uabaína endógena), y por lo tanto inhibidor de dicha bomba, que se ha encontrado elevada en un 45% de los pacientes con hipertensión arterial. La inhibición de la bomba resulta en un aumento del sodio intracelular miocárdico y arterial, agravando la hipertensión. De igual manera, en los túbulos proximales de las nefronas de los riñones, estimulan la bomba sodio/potasio, aumentando la reabsorción tubular y por consecuencia, la retención de sodio.
La relación de la uabaína (UB) con el sodio es diferente dependiendo de la ingesta y de la patología. En pacientes con tensión normal, la síntesis de UB se suprime ante una elevada ingesta de sal, evitando la inhibición de la bomba.
En hipertensos con elevada UB con ingesta normal de sodio, se observa hipertensión arterial por una inadecuada modulación de la síntesis de la sustancia digitálica o por falla en su depuración. En los pacientes hipertensos con elevación de la UB se produce un aumento significativo del tono arteriolar.
Por otra parte, el déficit de potasio estimula a diferentes transportadores tubulares renales de sodio, aumentando la reabsorción de sodio y por lo tanto la retención del mismo. Es decir, el potasio es reemplazado parcialmente por sodio, alterando la tonicidad y volumen de las células.
Además, el déficit de potasio estimula diferentes transportadores renales de sodio, como la bomba de sodio/potasio, acumulándose sodio, cuyo exceso hace que se elimine aún más potasio al influir sobre ciertos canales de potasio.
Por ende, una alimentación que contenga un exceso de sodio y un déficit de potasio incrementaría la aparición de la hipertensión arterial, tanto por aumentar la concentración y retención de sodio como por favorecer el déficit de potasio.
Otra implicación biomédica importante es la participación de esta bomba en la fisiopatología tiroidea. El exceso de la hormona tiroidea provoca una incrementación de la síntesis de la bomba de sodio potasio en las membranas, lo que deriva en un aumento de la tasa metabólica basal, que deriva en un aumento en el consumo de oxígeno, la frecuencia respiratoria, la temperatura corporal y la calorigénesis.
Bibliografía
- B. Carlos Zehnder,
Sodio, potasio e hipertensión arterial,
Revista Médica Clínica Las Condes,
Volume 21, Issue 4,
2010,
Pages 508-515,
ISSN 0716-8640,
https://doi.org/10.1016/S0716-8640(10)70566-6.
(https://www.sciencedirect.com/science/article/pii/S0716864010705666) - Pirahanchi Y, Jessu R, Aeddula NR. Fisiología, Bomba de Sodio Potasio. [Actualizado el 18 de marzo de 2022]. En: StatPearls [Internet]. Treasure Island (FL): Publicación de StatPearls; 2022 ene-. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK537088/
- https://psicologiaymente.com/neurociencias/bomba-sodio-potasio
- Zárate LH, Valenzuela A. Equilibrio sodio-potasio en la regulación de la hipertensión arterial. Medwave 2012 Feb;12(2) doi: 10.5867/medwave.2012.02.5301
- Educational resources supporting molecular explorations through biology and medicine. Christine Zardecki, Shuchismita Dutta, David S. Goodsell, Robert Lowe, Maria Voigt, Stephen K. Burley. (2022) Protein Science 31: 129-140 doi:10.1002/pro.4200
- Shinoda, T., Ogawa, H., Cornelius, F. et al. Crystal structure of the sodium–potassium pump at 2.4 Å resolution. Nature 459, 446–450 (2009). https://doi.org/10.1038/nature07939
- ChimeraX
- BioRender


